مقالات کیمیا رشد سپاهان
- همه
- تغذیه
- مقالات دامی
- مقالات طیور
سندرم افت تولید تخم مرغ (EDS)🥚آنچه مرغداران باید بدانند
سندرم افت تخم مرغ (EDS) که به عنوان سندرم کاهش تخم مرغ '76 نیز شناخته می شود، یک عفونت ویروسی است که مرغ های تخمگذار ...
گیاهان دارویی در تغذیه طیور: مزایا و محدودیت ها
گیاهان دارویی در تغذیه طیور نقش مهمی ایفا میکنند. این گیاهان دارای خواص درمانی و تغذیهای هستند که میتوانند به سلامت و بهرهوری طیور کمک ...
اهمیت ویتامین ها در تغذیه طیور: کلید سلامت و بهره وری بالا
ویتامینه ها مواد آلی کم مقداری هستند که برای رشد، تولید مثل، سلامت و عملکرد طبیعی طیور ضروری میباشند. ویتامین ها در جیره طیور در ...
مسمومیت در طیور: علائم و راههای درمان
مسمومیت در طیور اغلب با افزایش نرخ تلفات، کاهش ناگهانی سرعت رشد در گلههای گوشتی یا کاهش پارامترهای تولید در گلههای مولد و تخمگذار آغاز ...
بیماری نیوکاسل در طیور: علائم، تشخیص، درمان و پیشگیری
بیماری نیوکاسل یک بیماری ویروسی است که انواع مختلفی از پرندگان را تحت تأثیر قرار میدهد. این بیماری میتواند باعث کاهش تولید، کیفیت و سلامت ...
مسمومیت با مایکوتوکسین ها یا سموم قارچی در طیور
مایکوتوکسین ها ترکیبات سمی هستند که توسط گونه های خاصی از قارچ ها (کپک های سم زا) تولید می شوند. این سموم در صورت مصرف ...
تاثیر دامداری هوشمند بر تغذیه، تولید مثل و کیفیت دام
هدف دامداری هوشمند یا دامپروری دقیق (PLF) دستیابی به تغذیه بهتر، تولیدمثل بیشتر، افزایش کیفیت دام با استفاده از فناوری های دیجیتال و اینترنت اشیاء ...
آنفولانزای مرغی [علائم+پیشگیری+درمان]
آنفولانزای مرغی چیست؟ آنفولانزای مرغی گونهای بیماری ویروسی پرندگان است که ویروس عامل آن از خانواده Orthomyxoviridae میباشد. این ویروس خود دارای سه تیپ A,B،C است. ...
برونشیت مرغی [علائم+پیشگیری+ درمان]
برونشیت مرغی یک بیماری ویروسی است که جوجهها را تحت تاثیر قرار میدهد. این بیماری بسیار مسری و با سرعت انتقال بالا در گله پخش ...
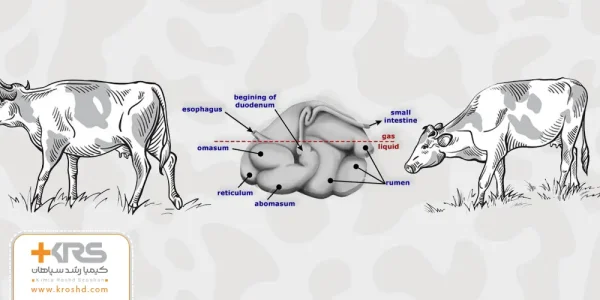
فیبر موثر فیزیکی در تغذیه نشخوارکنندگان (peNDF)
فیبر موثر فیزیکی در تغذیه نشخوارکنندگان (peNDF) از اهمیت زیادی برخوردار است. حفظ سلامتی دام و عملکرد مطلوب شکمبه و ایجاد شرایط مطلوب از نظر ...
الک پنسیلوانیا در تعیین یکنواختی TMR گاوهای شیری
در این فیلم طرز استفاده از الک پنسیلوانیا و محاسبات مربوط برای تعیین اندازه ذرات خوراک و یکنواختی TMRدر گاو شیری توضیح داده شده است.
پیکا در گاوهای شیری 🐮[علت + بهترین روش درمان]
پیکا یا اشتهای بیهوده به خوردن مواد غیر مغضی در گاوهای شیری، این گاوها تمایل زیادی به خوردن شن، ماسه، بستر کثیف، ادرار می باشد. ...
5 معیار کلیدی برای ارزیابی کیفیت توکسین بایندر
کیفیت توکسین بایندر یعنی ظرفیت اتصال به سموم به دلیل ساختار متنوع جاذب و تنوع بین مایکوتوکسین ها میتواند از محصولی به محصول دیگر به ...
استرس گرمای در گاو (تنش گرمایی در گاو) : کاهش و مدیریت
استرس گرمایی در گاو (تنش گرمایی در گاو) زمانی رخ می دهد که مقدار گرمایی که گاو از طریق تعریق، تنفس، همرفت و… دفع می ...
پرورش گوساله شیرخوار ⭐ [نکات طلایی]
در گاوداری های تجاری پرورش گوساله شیرخوار ، گوساله معمولاً طی ۲۴ ساعت اول پس از زایمان از مادر جدا میشود و تا زمان شیرگیری ...
رفتار شناسی گاو
طبیعی بودن به عنوان یکی از سه حوزه آسایش دام، از نظر مفهومی مبهم ترین و مسلماً چالش برانگیزترین موضوع در صنعت پرورش گاو شیری ...
توکسین بایندر در تغذیه دام و طیور
توکسین بایندر از نظر تغذیه ای ماده بی اثری است که به خوراک اضافه می شود تا به مایکوتوکسین ها در دستگاه گوارش متصل شود ...
بافر دامی (مکمل بافری) در جیره گاوهای شیری
بافر دامی با افزایش غلظت اسید در شکمبه مقابله می کند و مقاومت شکمبه در برابر تغییر اسیدیته هنگام مصرف جیره هایی با کنسانتره بالا ...
مکمل ویتامینه و معدنی دام: کاهش هزینه جیره
مکمل ویتامینه و معدنی دام مصرف مکمل ویتامینه و معدنی دام به عنوان یک ابزار مدیریتی برای پشتیبانی ازسطح تولید بالا، بهبود عملکرد تولید مثلی ...
مکمل دامی مناسب گله شما کدام است؟
مکمل دامی به عنوان مهمترین جزء از بخش کنسانترهای جیره و ترکیبی از مواد مغذی است. انواع مکمل دامی علاوه بر تامین کمبودهای موجود در ...
سیستم ایمنی پرندگان
سیستم ایمنی بخش مهمی از بدن هر موجود زنده بوده که از آن در برابر عوامل بیماریزای موجود در محیط (ویروسها، باکتریها، انگلها و…) و ...







![آنفولانزای مرغی [علائم+پیشگیری+درمان] آنفولانزای مرغی [علائم+پیشگیری+درمان]](https://kroshd.com/wp-content/uploads/elementor/thumbs/bird-flu-H5N1-1-qimroojkxdesrhp7kx6gqlivg230gr3cf8ymr8quns.webp)
![برونشیت مرغی [علائم+پیشگیری+ درمان] برونشیت مرغی [علائم+پیشگیری+ درمان]](https://kroshd.com/wp-content/uploads/elementor/thumbs/Infectious-Bronchitis-in-Chickens-1-qh88f5kypxpkpqp9rzfsqnsyhbc9bkbxwdzyucnfeg.webp)


![Pica in dairy cows پیکا در گاوهای شیری [علت + بهترین روش درمان]](https://kroshd.com/wp-content/uploads/elementor/thumbs/Pica-in-dairy-cows-1-qeklrl4knv9dza12g5ik1dbqstzbi0pt0a2yx15igo.webp)